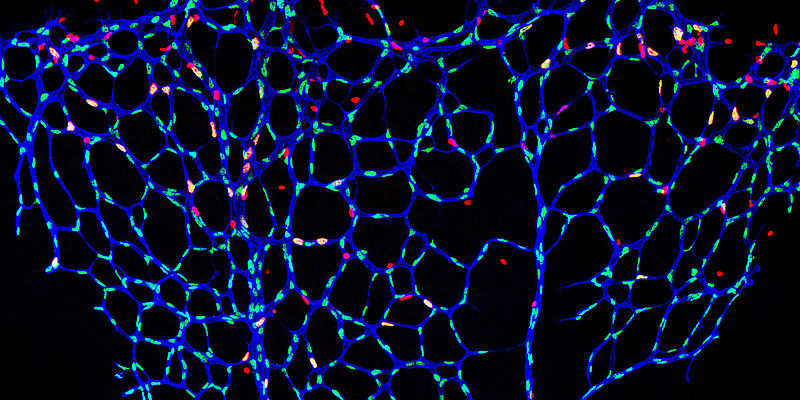
Erkrankungen des Herz-Kreislauf-Systems stehen häufig mit einer gestörten Funktion der Blutgefäßinnenhaut (Endotheldysfunktion) in Verbindung. Die Arbeitsgruppe von Univ.-Prof. Dr. Philip Wenzel, Stellvertretender Direktor der Kardiologie I im Zentrum für Kardiologie der Universitätsmedizin Mainz und Principal Investigator am DZHK, hat entdeckt, dass das Protein Tubulin-folding cofactor E (TBCE) eine entscheidende Rolle dabei spielt. TBCE gehört zu den Proteinen, die wichtig sind, um den Zellen Struktur und Form zu geben und damit die normale Funktionsweise ermöglichen.
Wirkstoff kann Stressreaktionen im Gefäß unterbinden
Die Forscher konnten zeigen, dass ein Mangel oder eine Mutation des Proteins TBCE zu einer Stressreaktion in der Gefäßwand führt. Betroffen ist dabei das endoplasmatische Retikulum, das innere Netzwerk der Zellen. Der vaskuläre Stress geht unter anderem mit Entzündungen und vermehrter Gefäßsteifigkeit einher.
Aus Vorstudien war bekannt, dass der Wirkstoff TUDCA (Tauroursodeoxycholic acid; Tauroursodeoxycholsäure) Stressreaktionen im endoplasmatischen Retikulum unterbinden kann. Im Rahmen der Mainzer Studie verbesserte sich die Endothelfunktion im Tiermodell durch eine gezielte pharmakologische Therapie mit TUDCA, auch wenn das Protein TBCE defekt war.
„Die aktuell publizierte Arbeit zeigt das Potential, am Biotechnologie-Standort Mainz mit strategischem Einsatz von Forschungsmitteln wichtige Erkenntnisse zu gewinnen, die einen unmittelbaren Vorteil für die Gesundheitsfürsorge der Menschen haben können“, betont Univ.-Prof. Dr. Thomas Münzel, Direktor der Kardiologie I im Zentrum für Kardiologie der Universitätsmedizin Mainz.
Störungen des Endothels sind Nährboden für Atherosklerose
Das Endothel ist die Innenhaut der Blutgefäße und bespannt wie eine feine Membran aus spezialisierten Zellen das Gefäßbett im ganzen Körper von innen. Es sorgt für die Weit- und Engstellung der Gefäße und damit für einen geregelten Blutfluss im Körper. Störungen des Endothels sind damit der Nährboden für Atherosklerose, Koronare Herzerkrankung, Herzinfarkt und Schlaganfall sowie für Thrombosen und Lungenembolien. Zusätzliche Faktoren wie Rauchen und Bluthochdruck können die endotheliale Dysfunktion verstärken.
Die ersten Hinweise auf den jetzt neu entdeckten Mechanismus zur Regulation der Blutgefäßfunktion ergab die Auswertung von genetischen Daten aus der Gutenberg-Gesundheitsstudie (GHS). In der Studie der Universitätsmedizin Mainz werden seit rund 14 Jahren Daten zu Risikofaktoren von Herz-Kreislauf-Erkrankungen in der Bevölkerung der Rhein-Main-Region gesammelt und zusammen mit molekularbiologischen Messungen erfasst. „Es ist faszinierend zu sehen, dass die GHS in der Lage ist, diese Informationen zu liefern“, berichtet Univ.-Prof. Dr. Philip Wenzel.
Ergebnisse können Basis für neue Therapie der Endotheldysfunktion sein
„Durch unser experimentelles Know-how war es darüber hinaus möglich, aus den komplexen Daten eine bisher unbekannte Funktionsweise herauszuarbeiten. Unsere Forschungsergebnisse zu TBCE liefern vielversprechende Hinweise, dass dieser Mechanismus medikamentös beeinflusst werden kann, um die Gefäßfunktion bei den betroffenen Patienten zu verbessern. Dies ist insbesondere deshalb von großer Bedeutung, weil die bisherige Therapie der Endotheldysfunktion mit Vitaminen oder Spurenelementen nur unzureichende Erfolge zeigt“, erläutert Professor Wenzel.
Originalpublikation:
Efentakis et.al Tubulin-folding cofactor E deficiency promotes vascular dysfunction by increased endoplasmic reticulum stress. Eur Heart J. 2021 Jun 16:ehab222.