Bluthochdruck steht ganz oben auf der Rangliste der chronischen Gesundheitsprobleme: Rund ein Drittel der Weltbevölkerung ist betroffen, in Deutschland sogar knapp 44 Prozent der Bürgerinnen und Bürger. Ist der Druck in den Blutgefäßen erhöht, leiden die Organe des Körpers, allen voran, das Gehirn, das Herz und die Gefäße. Das steigert nicht nur das Risiko für schwerwiegende Herzkreislauferkrankungen wie Schlaganfall oder Herzinfarkt. Herz, Hirn und Gefäße sind im gesunden Körper auch maßgeblich daran beteiligt, den Blutdruck zu regulieren. Nehmen sie durch dauerhaften Bluthochdruck Schaden, verlieren sie diese Fähigkeit – ein Teufelskreis.
Damit der Blutdruck wieder sinkt, sollten Betroffene zuerst ihren Lebensstil umstellen: sich ausgewogen und salzarm ernähren, regelmäßig Sport treiben und aufs Rauchen verzichten. Auch verschiedene Medikamente wie Beta-Blocker oder ACE-Hemmer können helfen: „Herkömmliche Medikamente können zwar den Blutdruck senken, bei vielen Betroffenen erreicht man damit aber nicht die erhoffte Schutzwirkung für die Organe“, sagt Dr. Suphansa Sawamiphak, Leiterin der Arbeitsgruppe „Kardiovaskulär-Hämatopoetische Interaktionen“ am Max Delbrück Center. Das werde im Gehirn besonders deutlich, wo bei Bluthochdruck feine Blutgefäße durchlässig werden oder absterben. „Demnach muss es im Gesamtgeschehen noch weitere Schaltstellen geben, die wir mit konventionellen Wirkstoffen nicht erreichen.“
Schon länger ist bekannt, dass Bestandteile des Immunsystems hier eine Rolle spielen könnten. Entzündungsreaktionen im Körper tragen zum Bluthochdruck bei und ziehen Organe in Mitleidenschaft. Wie das im Detail abläuft, ist bislang nicht bekannt.
Immunzellen schädigen Blutgefäße im Zebrafisch-Gehirn
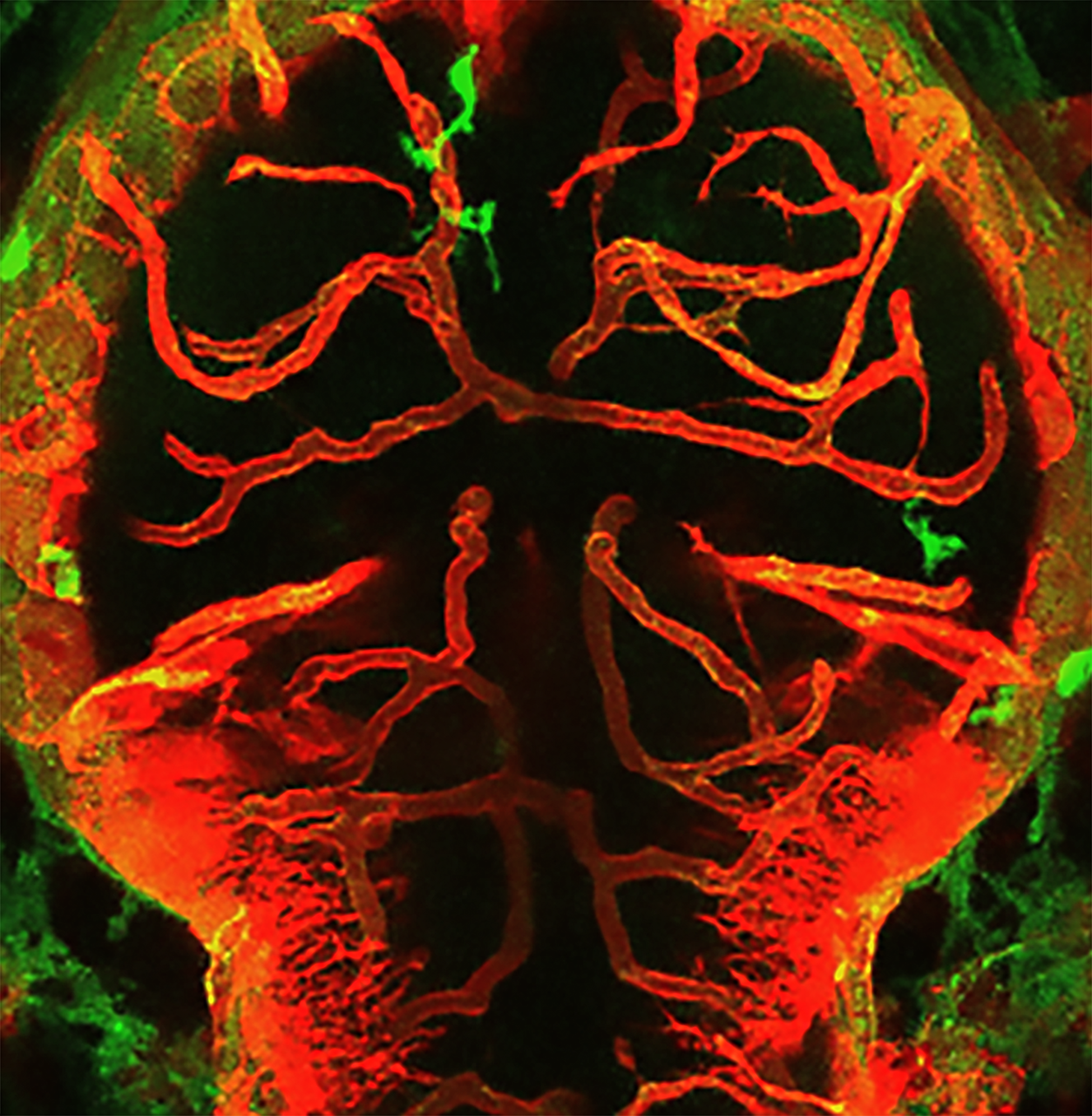
Um den verantwortlichen biologischen Mechanismen auf den Grund zu gehen, untersuchte Sawamiphak zusammen mit ihrem Team am Max Delbrück Center und Kolleg*innen aus Italien und der Schweiz Larven des Zebrafisches. „Das ist ein sehr gutes Modellsystem für viele Fragestellungen, weil wir die Tiere durch Veränderung der Umgebung leicht manipulieren können“, sagt die Biologin und erklärt weiter: „Weil junge Zebrafische durchsichtig sind, können wir die Auswirkungen am lebenden Tier beobachten.“
Um nun die Rolle des Immunsystems bei Bluthochdruck zu analysieren, haben die Forschenden Zebrafischlarven im Wasser mit niedriger Ionenkonzentration aufgezogen. Dadurch entsteht bei den Tieren ein Ionenungleichgewicht im Körper, das vergleichbar ist mit übermäßigem Salzkonsum beim Menschen und das zu Bluthochdruck führt. Anschließend haben sie untersucht, welche Auswirkungen dies auf die Blutgefäße im Gehirn hat.
Nach den Beobachtungen der Forschenden führt Bluthochdruck zu mehr Makrophagen und Mikroglia, spezielle Immunzellen des Gehirns, die vermehrt auf Gefäßoberflächen treffen können. Sie treten dort mit dem Endothel in Kontakt, der Zellschicht, die die Blutgefäße von innen auskleiden, und schwächen die Gefäßwände zunehmend. Auch die Blut-Hirn-Schranke, die das Gehirn vor schädlichen Substanzen und Krankheitserregern schützt, nimmt Schaden. „Das Interessante ist, dass Makrophagen und Mikroglia bei gesundem Blutdruck normalerweise die Gefäße schützen“, sagt Sawamiphak. „Unsere Ergebnisse deuten darauf hin, dass Makrophagen beziehungsweise Mikroglia bei Bluthochdruck regelrecht umprogrammiert werden.“
Blockiert man den Botenstoff, treten keine Organschäden auf
Eine wichtige Rolle spielen dabei Entzündungsbotenstoffe wie IFN-Gamma, die unter Bluthochdruckbedingungen vermehrt ausgeschüttet werden. Um diesen Zusammenhang experimentell zu untermauern, schalteten sie das Gen für einen Rezeptor aus, an den IFN-Gamma normalerweise bindet. Bei diesen Fischen hinterließ der Bluthochdruck keine Schäden in Blutgefäßen und Bluthirnschranke. Auch bei Mäusen gelang dem Team der Nachweis, dass Wirkstoffe, die IFN-Gamma hemmen, typische Begleiterscheinungen von Bluthochdruck – darunter Schäden der Blut-Hirn-Schranke, Abbau der Blutgefäße im Gehirn sowie kognitive Defizite – verhindern können.
„Unsere Ergebnisse eröffnen eine völlig neue Perspektive auf die Rolle von Entzündungsvorgängen bei der Entstehung von Bluthochdruck“, unterstreicht Sawamiphak die Bedeutung ihrer Arbeit. Nun gelte es, die beteiligten Immunzellen und Immunmodulatoren genauer zu charakterisieren und ihre Rolle bei höheren Tieren bis hin zum Menschen zu überprüfen. Sollte sich dies bestätigen, hätte das Team mit dieser Studie neue Angriffspunkte für die Therapie bei Bluthochdruck gefunden. Davon würden insbesondere Betroffene profitieren, bei denen herkömmliche Wirkstoffe nicht vor zunehmenden Organschäden zu schützen vermögen.
Originalpublikation: Dilem C Apaydin, Bhakti I Zakarauskas-Seth et al. (2023): Interferon-γ drives macrophage reprogramming, cerebrovascular remodeling, and cognitive dysfunction in a zebrafish and a mouse model of ion imbalance and pressure overload. Cardiovascular Research, doi: 10.1093/cvr/cvac188
Wissenschaftliche Ansprechpartnerin: Dr. Suphansa Sawamiphak, Leiterin der Arbeitsgruppe Kardiovaskulär-Hämatopoetische Interaktionen, Max Delbrück Center, Suphansa.Sawamiphak(at)mdc-berlin.de