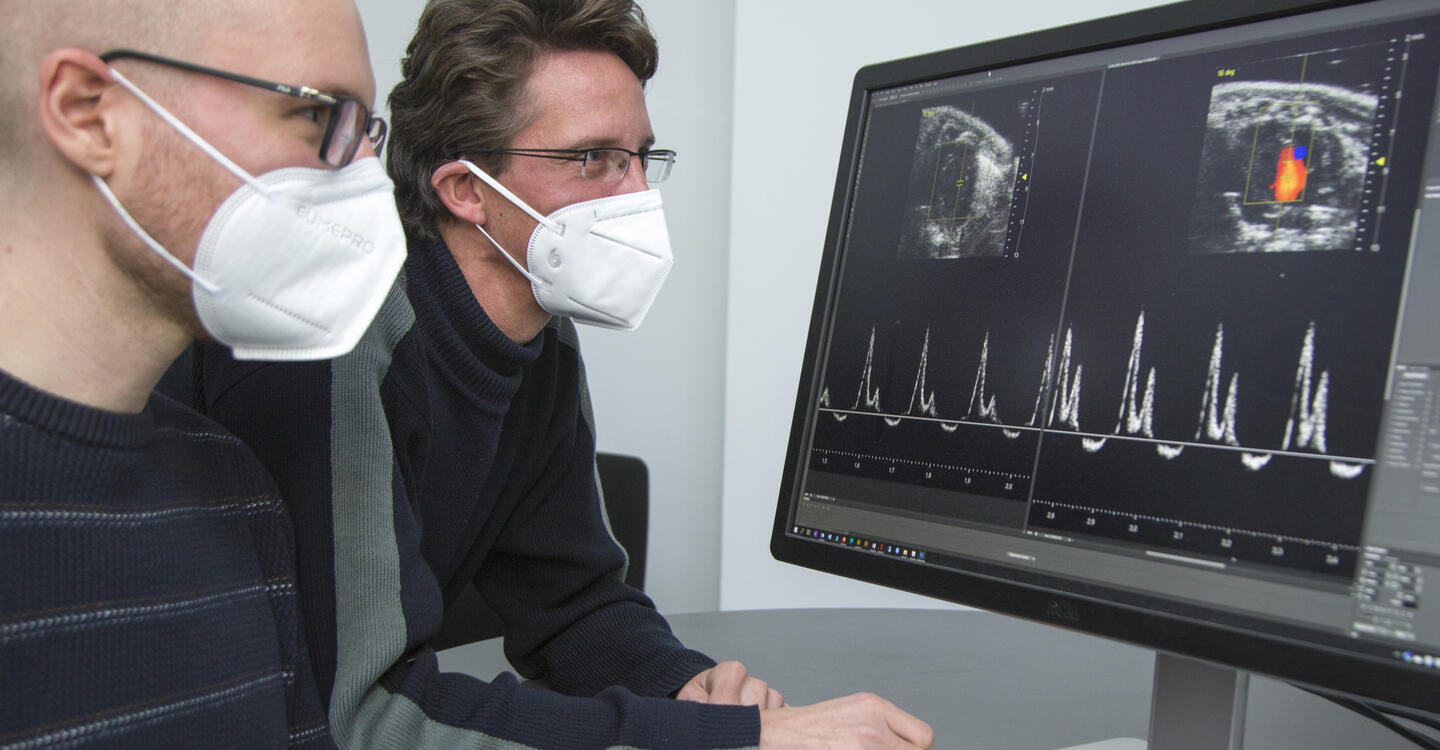
Bei Mäusen und in künstlich hergestelltem menschlichem Herzgewebe funktioniert es schon: Ein Wirkstoff, den ein Team um DZHK-Wissenschaftler Professor Michael Gotthardt vom Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) entwickelt habt, bringt „neuen Schwung“ in schwache Herzen.
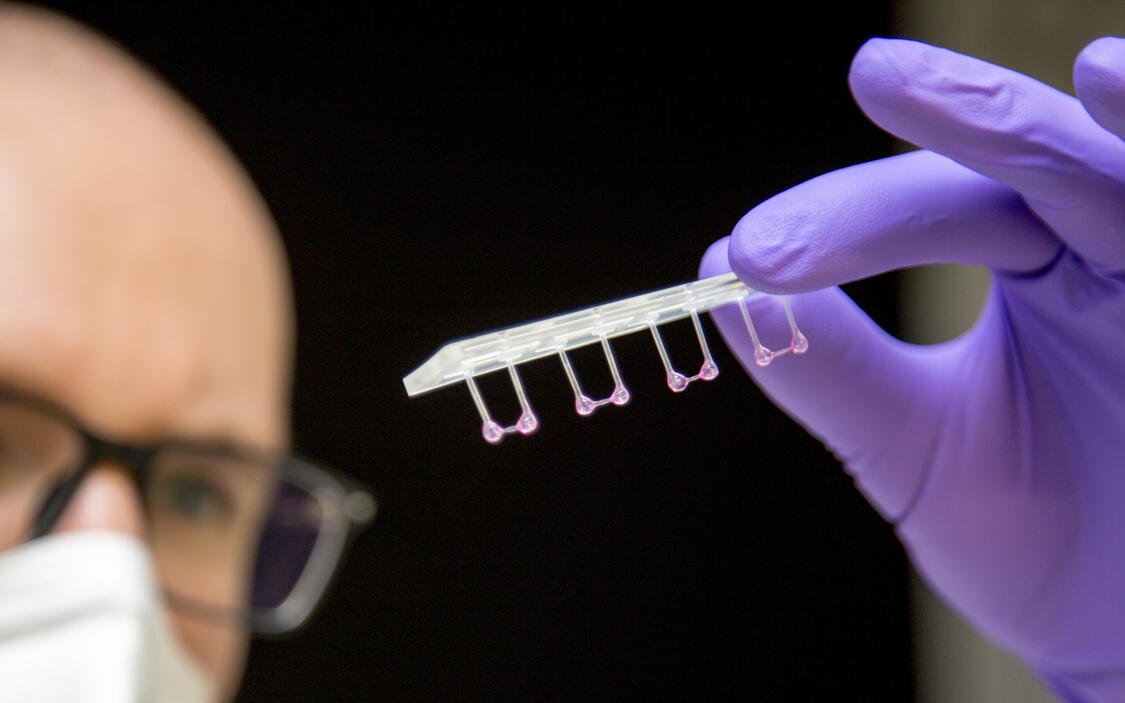
Antisense-Oligonukleotiden – kurz: ASOs – heißt der Wirkstoff, bei dem es sich um eine synthetisch hergestellte Nukleinsäure handelt und der Hoffnung macht auf eine neue, medikamentöse Therapie. Denn für eine Form der Herzschwäche, die Herzinsuffizienz mit erhaltener Pumpfunktion (HFpEF), gibt es bislang kaum wirksame Behandlungsmöglichkeiten.
Die Symptome der beiden Formen von Herzinsuffizienz gleichen sich: Patienten und Patientinnen sind oft kurzatmig und schnell erschöpft. Sie leiden häufig unter Wassereinlagerungen, Herzrasen und Schwindel. Anders als bei der bereits gut behandelbaren Herzschwäche mit reduzierter Pumpfunktion ist die Pumpkraft des Herzens bei HFpEF noch erhalten. Die linke Herzkammer ist jedoch steif und wird nicht mehr ausreichend mit Blut gefüllt.
Mit Hilfe von ASOs können die Forscher nun einen bestimmten Vorgang, das alternative Spleißen, so beeinflussen, dass vermehrt elastische Titine gebildet werden. Titin-Proteine beeinflussen die Elastizität des Herzens. Sie werden von Herzmuskelzellen in unterschiedlichen Varianten produziert: von sehr elastisch bis steif. Bei Herzschwäche mit erhaltener Pumpfunktion können unter anderem steifere Titine dazu führen, dass sich die linke Herzkammer nicht mehr gut mit Blut füllt.
Mehr Elastizität fürs kranke Herz
„Die mechanischen Eigenschaften der Titine sind nur schwer zu beeinflussen. Aber wir können jetzt in den Prozess eingreifen, der der Proteinsynthese vorausgeht – das alternative Spleißen“, sagt Michael Gotthardt. Alternatives Spleißen ist ein raffinierter Trick der Natur, um auf Basis eines einzelnen Gens eine Vielfalt ähnlicher Proteine zu bilden – so auch die verschiedenen Formen des Titins. Kontrolliert wird dieser Prozess durch Spleißfaktoren. „Einer davon, der Masterregulator RBM20, ist ein geeignetes Ziel, das wir therapeutisch angehen können“, erklärt Michael Gotthardt. RBM20 bestimmt die elastischen, kontraktilen und elektrischen Eigenschaften der Herzkammern.
Die Forscher suchten nun nach einem Weg, RBM20 zu beeinflussen. „Wir waren überrascht, wie einfach dies möglich ist“, sagt Gotthardt – nämlich mit Antisense-Oligonukleotiden, also ASOs. Der Antisense-Wirkstoff schaltet RBM20 ab. Mit dem Effekt, dass sich mehr elastisches Titin bildet.
Bei Mäusen mit steiferen Herzwänden haben die Wissenschaftler ASOs bereits erfolgreich getestet. Auch in künstlichem Herzgewebe aus menschlichen Stammzellen zeigte sich der gewünschte Effekt.
An der Therapieform sei noch zu arbeiten, so Michael Gotthardt. „Schöner als eine wöchentliche Spritze, die viele Patientinnen und Patienten bereits von Insulin oder Heparin kennen, wäre eine orale Form.“
Publikation: Therapeutic inhibition of RBM20 improves diastolic function in a murine heart failure model und human engineered heart tissue. Radke, Michael H. et al. (2021). Science Translational Medicine DOI: 10.1126/scitranslmed.abe8952
Quelle: Pressemitteilung MDC
Diese wissenschaftliche Publikation wurde vom DZHK-Vorstand zum Paper of the Month Dezember 2021 gewählt.