Eine krankhafte Zunahme der Herzmuskelmasse gilt als die häufigste Ursache für den plötzlichen Herztod. Aber wie kommt es zur Herzhypertrophie? Wissenschaftler haben einen komplexen molekularen Mechanismus entschlüsselt, der die gesamte Proteinproduktion in den Ribosomen der Herzzellen stört. Das Herz bekommt nicht die Eiweiße, die es eigentlich braucht was letztlich zu einem abnormen Wachstum der Herzmuskelzellen führt.
Natürliche genetische Abweichungen beeinträchtigen gesamte Eiweißproduktion
Überraschend für die 19 Forschenden aus sechs Ländern war, dass es genetische Variationen gibt, die sich auf die komplette Proteinproduktion in den Ribosomen des Herzgewebes auswirken. Ribosomen sind die zellulären Eiweißfabriken des Körpers. Ein Team um Professor Norbert Hübner vom Berliner Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) hat an der Studie mitgearbeitet. Hübner ist Principal Investigator am DZHK.
Bekannt ist bereits, dass Abweichungen im Erbgut beeinflussen können, ob und wie die Gene im Zellkern abgelesen werden. Dieser Transkription genannte Prozess ist der erste Schritt auf dem Weg zur Proteinherstellung. Ebenso bekannt sind Veränderungen der DNA, die dazu führen, dass einzelne Proteine des Herzens fehlerhaft hergestellt werden. Neu hingegen ist, dass Variationen im Erbgut die gesamte Proteinsynthese, also die Herstellung der Proteine, schädigen können.
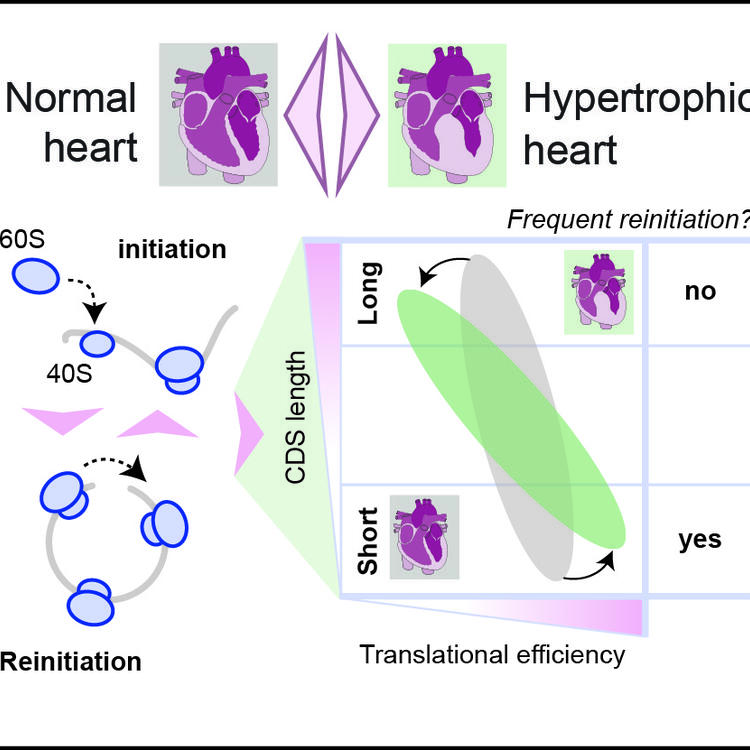
Bei Ratten mit Herzhypertrophie stieß das Team auf eine veränderte Region im Genom. Die genetische Variation wirkt sich auf lange und kurze Proteine unterschiedlich stark aus. Die Produktion des wichtigen Muskeleiweißes Titin beispielsweise, ein langes Protein, leidet darunter. Das wiederum wirkt sich nachteilig auf den Aufbau der Sarkomere aus, die kleinste funktionelle Einheit der Muskelfaser und führt letztendlich zu einer Verdickung der Herzkammern und zu Herzversagen.
Entdeckung liefert Hinweis darauf, wie komplexe Krankheiten entstehen können
„Besonders bemerkenswert ist, dass ähnliche Erbgutvariationen auch bei anderen Arten – etwa bei Mäusen, Menschen und sogar bei einzelligen Organismen wie der Hefe – die gleichen Effekte auf die Proteinsynthese haben“, berichtet Hübner. Das zeige, wie verbreitet der genetisch bedingte Defekt in den Proteinfabriken der Zellen sei, wie wenig er sich im Laufe der Evolution verändert habe und wie wichtig er für die Entstehung komplexer Krankheiten, die auch den Menschen betreffen, sei.
„Der von uns entschlüsselte Mechanismus könnte womöglich erklären, warum manche Menschen genetisch prädisponiert sind, Herzhypertrophie zu entwickeln“, sagt Hübner. „Darüber hinaus legt unsere Arbeit den Grundstein für zukünftige Studien zur genetischen Veranlagung für komplexe Krankheiten, die auch andere Organe als das Herz betreffen können.“
Originalpublikation: Franziska Witte, Jorge Ruiz-Orera et al. (2021): „ A trans locus causes a ribosomopathy in hypertrophic hearts that affects mRNA translation in a protein length-dependent fashion“. Genome Biology, DOI: 10.1186/s13059-021-02397-w
Quelle: Pressemitteilung des Max-Delbrück-Centrums für Molekulare Medizin